重症监护病房中罕见的呼吸系统疾病:何时怀疑和如何处理

翻译:王剑荣 校对:王剑荣

本文目的
为了开始有针对性的治疗,需要迅速确定急性呼吸衰竭(ARF)/急性呼吸窘迫综合征(ARDS)的原因。然而,约10%的ARDS患者在诊断时没有发现ARDS危险因素。在这种背景下,已经报告了许多罕见的ARF原因。这篇综述的目的是介绍ARF/ARDS的主要的罕见原因,并为临床医生提供实用的诊断方法。
近期发现
最近的流行病学数据提出了鉴别非暴露于常见危险因素的ARDS患者亚组的方法。这些可以归类为:免疫、药物诱导、恶性和特发性疾病。标准化的诊断检查包括胸部成像,客观评估左心充盈压,支气管肺泡灌洗液微生物学检查和细胞学分析,免疫学检查以及寻找肺毒性药物,这些可以在大多数情况下确定ARF的病因。在其他情况下,应考虑进行开胸肺活检。
总结
需要迅速确定ARF的病因才能启动靶向治疗。没有确定ARDS危险因素的患者应接受全面、分级的诊断检查。
关键字
急性呼吸窘迫综合征,柏林定义,诊断技术和程序,预后
背景
急性呼吸衰竭(ARF)是ICU入院的主要原因之一,ICU入院的患者中有10%符合全球性lung safe研究中的急性呼吸窘迫综合征(ARDS)的标准。尽管需要立即获得呼吸支持以保持气体交换并防止病情恶化,我们仍需要迅速查明ARF的病因,以便开始进行早期目标性治疗。然而,在极少数情况下,在进行了初步诊断努力后,仍然难以确定ARF的原因。对这类患有ARF罕见病因的患者进行治疗对重症医生而言是一个挑战,因为据报道,最终没有确诊的患者存活率较其他患者低。本文主要回顾了以下临床场景:治疗没有明确原因的低氧性ARF(达到或未达到ARDS标准)的患者时应怀疑的主要疾病,以及应考虑的诊断方法和治疗方法。这篇综述将侧重于涉及肺实质的罕见疾病,但不会涉及导致ARF的气道、血管、神经肌肉或胸壁疾病。
关键点
1、约有10%的急性呼吸道疾病患者窘迫综合征(ARDS)在ARDS诊断中没有发现常见的危险因素。
2、ARDS缺乏常见危险因素的原因包括:免疫,药物诱导,恶性和特发性原因。
3、当前的建议支持及时开始对免疫源性ARDS进行免疫抑制治疗。
4、对这些因罕见原因导致急性呼吸衰竭病人的管理需要采用多学科方法。
急性呼吸衰竭和急性呼吸窘迫综合征的罕见原因
在先前的大规模研究中已全面报道了ARDS的主要病因,主要包括肺炎(59%),肺外的脓毒症(16%),胃肠误吸(14%),非心源性休克(7%)和多发性创伤(4%)。这些原因在2012年柏林定义中被列为ARDS的“常见”危险因素。然而,有一些病例系列报告ARDS患者的肺组织病理,包括死亡后和活检的,都显示出ARDS的不常见原因相对频繁(达到三分之一的患者)。事实上,在从符合ARDS柏林定义标准时死亡的患者中获得的大量肺组织学研究中,除弥漫性肺泡损伤(即ARDS 的以往的组织学标志)以外的其他诊断的病例很多,包括肺纤维化(自身免疫或药物诱导),弥漫性肺泡出血,机化性肺炎,甚至肺肿瘤浸润。几种临床特征可以帮助临床医生怀疑这种不寻常的诊断:包括自身免疫/结缔组织病的既往病史或暴露于已知的肺毒性药物、亚急性起兵的症状(即自>7天起且<30天出现的呼吸道症状)、存在肺外症状、或没有任何微生物学证据的情况下,经过充分的抗生素治疗肺炎仍未好转。重要的是,7天内开始出现呼吸道症状(即符合柏林定义的时间标准)尽管特异性不足,不应是临床医生排除特殊病因的理由。一个可能有助于临床医生怀疑非典型病因的简单线索是缺乏可确定的导致ARDS的危险因素。Gibelin等进行的研究报告说,有7.5%的ARDS患者未发现常见的危险因素。令人惊讶的是,这一数据在LUNG SAFE研究的辅助分析中得到了证实,该分析证实了大约8%的ARDS患者在确诊ARDS时并未发现ARDS的常见危险因素,重要的是,柏林ARDS定义强调指出,当未确定ARDS危险因素时,应进行左心充盈压的客观评估,以排除对静水型肺水肿的诊断。
支气管肺泡灌洗液(BAL)和CT扫描虽然经常显示出不明确的发现,但可能有助于怀疑ARF/ARDS的罕见原因(表1),如本综述以下的诊断方法所述。
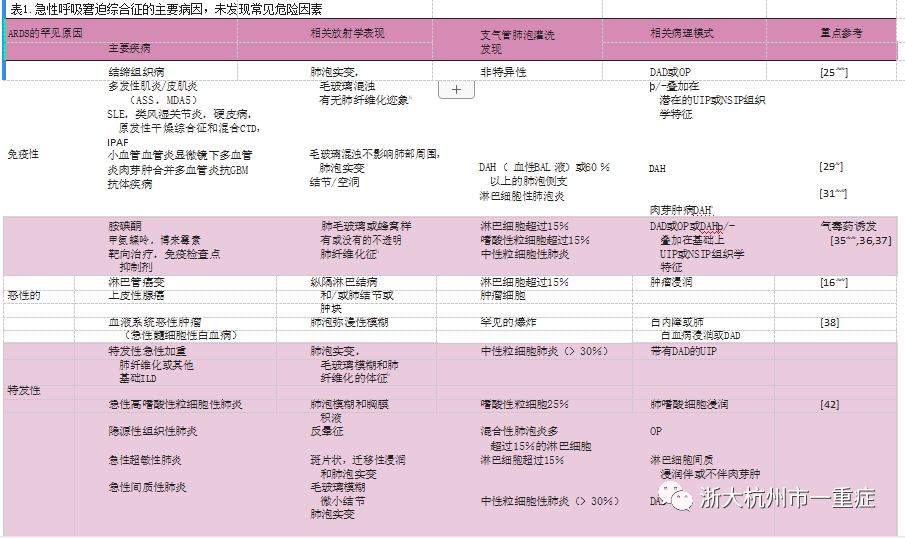
尽管提供可能导致ARDS的罕见疾病的完整列表超出了本文的范围,但表1根据专家的意见和病例研究,提供主要疾病的实用列表,这些病因可以归为四类 ARF / ARDS的罕见原因,如下:免疫、药物诱导和恶性原因以及特发性疾病。
免疫原因
结缔组织疾病( CTD)是ARF的主要免疫原因类别。其中,多肌炎/皮肌炎的肺部表现是最典型的,表现为较差的预后和更高的死亡率,多发性肌炎/皮肌炎是一组罕见的CTD,表现为不同程度的肌肉炎症。抗氨基酰基tRNA(ARS)合成酶抗体的存在,与肌炎或间质性肺疾病一起被称为抗合成酶综合症,也常常与发烧,机械手和雷诺现象相关。已经鉴定出总共八种ARS抗体,其中最常见的是抗Jo1抗体,在大多数抗合成酶综合症和多达三分之一的炎症性肌病中能碰到。除ARS抗体外,2005年在临床上患有肌病性皮肌炎的患者中还发现了抗MDA-5抗体,因此最初被称为抗CADM抗体。抗MDA-5抗体描述了特殊的临床情况。模仿抗合成酶综合症的表型。然而,抗MDA-5抗体的存在使死亡(主要是呼吸道原因)的风险大大增加。
实际上,Vuillard等最近报道了多中心队列的抗合成酶或抗MDA-5抗体的患者出现需要ICU入院的ARF,并表明尽管积极处理,后者的医院死亡率却比前者高得多(84比29%)。其他偶尔出现导致ARF的间质性肺疾病的CTD包括类风湿性关节炎、硬皮病、原发性干燥综合征和混合CTD 。系统性红斑狼疮(有或没有抗磷脂综合征)可由于与肺毛细血管炎有关的弥漫性肺泡出血而导致严重而突然出现ARF,在三分之二以上的病例中伴有急性肾小球肾炎,可表现为这种疾病。具有自身免疫特征的间质性肺炎(IPAF)是欧洲呼吸学会/美国胸科学会工作组最近提出的一个新名词,用于将患有特发性间质性肺炎的患者与某些提示自身免疫过程的临床特征进行分类(肺外症状或血清自身抗体阳性),但不符合任何特定CTD的既定标准。需要进行前瞻性研究以确定IPAF患者的预后,有趣的是,Grasselli等最近发表了一个病例系列,其中7例ARDS患者缺乏柏林定义的常见危险因素,最终归类为IPAF,其中5例从ICU转出。
需要入ICU的ARF可能情况比较复杂,多达90%的病例中显示小血管血管炎,主要是多血管炎和显微镜检性多血管炎的肉芽肿病。患者可能散发出现的ARF(约三分之一的病例),通常与弥漫性肺泡出血(DAH)有关,或出现肺肾综合征(约三分之一的病例),定义为DAH与迅速进展性肾小球肾炎。需要迅速鉴别患有血管炎苗头的患者,以开始有针对性的治疗,并防止ARF恶化和肾功能恶化,这可能导致肾脏坏死。与间接免疫荧光法相比,现在推荐使用高质量的蛋白酶3和髓过氧化物酶-ANCA免疫测定法进行抗中性粒细胞胞浆抗体(ANCA)检测,作为首选的首选筛查方法,并且对某些患者具有较高的诊断率。
抗肾小球基底膜(GBM)抗体疾病是DAH的罕见原因通常表现为肺肾综合征。可用ELISA法在90%以上的患者中检测到循环中的高特异性抗GBM抗体。但是,医生应意识到测试的阴性结果可能是由于所有抗体都在其靶标(肺和肾)上或缺乏敏感性。在后一种临床情况下,可以进行肾脏活检,通常表现为毛细血管外肾小球肾炎,免疫球蛋白G沿GBM呈线性沉积。需要紧急免疫抑制和血浆置换以防止肾脏功能的永久性丧失。
药物引起的原因
据报道,很多种类的药物是药物诱发的肺炎的病因,可能导致ARF/ ARDS。Dhokarh等报道,在514名ARDS患者的回顾性队列中,其中9.5%可归类为药物引起的ARDS 。在Gibelin 等人的研究中。最终确定患有ARDS且没有共同危险因素的ARDS患者的26%(占整个队列的7.5%)被诊断为药物诱发的ARDS,主要归因于化疗药物和胺碘酮。实际上,所有药物都可能与肺部副作用有关,具有各种各样的临床和放射学特征(间质性肺疾病,ARDS,DAH,嗜酸性粒细胞性肺炎),这对临床医生的诊断尤其具有挑战性。在这种情况下,药物引起的呼吸系统疾病网站(pneumotox.com)可能是有用的工具。发生肺毒性风险较高的患者包括年龄较大、既往肺疾病的患者(包括间质性肺疾病,肺外科手术或肺癌)。
近几年来,免疫检查点抑制剂代表了肿瘤学的最新突破,可产生免疫相关的不良事件,包括间质性肺疾病,可能导致ARF。Delaunay等报告说,接受免疫检查点抑制剂(主要是PD-1抑制剂)的患者中有3.5 % 被诊断为药物诱发的间质性肺病。在Naidoo等人的最新研究中,应用抗细胞毒性T淋巴细胞-4单抗联合治疗进一步增加了发生肺炎的风险。酪氨酸激酶抑制剂,包括克罗替尼,在间变性淋巴瘤激酶重排的非小细胞肺癌中抑制病情进展的药物,也已被确定为药物性间质性肺病的病因。鉴于这些药物的使用量日益增加,将来将需要临床医生加强这些意识。
恶性原因
ARF可以发现各种肿瘤,并符合ARDS的临床和放射学标准,主要包括实体淋巴管癌和肺腺癌。胸部CT扫描时发现纵隔/肺门淋巴结病变和/或肺结节或肿块将有助于提高临床怀疑并指导诊断策略。在血液系统恶性肿瘤中,急性髓细胞性白血病可导致三种特定的白血病症状:肺白细胞减少,肺白细胞浸润和急性细胞溶解性肺炎,28天死亡率达到34%。
特发性病因
急性间质性肺炎是指一种特发性ARF,在组织学上具有急性或组织性DAD的特征,尽管没有暴露于ARDS危险因素,也未发现其他原因,包括CTD和药物暴露。该病会影响各个年龄段、性别的患者,并且通常会先感冒样流感。症状持续时间在病例系列中为2到11天。在特发性肺纤维化(IPF)/通常为间质性肺炎(UIP)的急性加重患者中发现的体格检查发现是非特异性的。尽管仅有少量证据支持,治疗仍依赖支持治疗和大剂量静脉内类固醇治疗。据报道,在先前的病例系列中死亡率为50%至100%。隐源性机化性肺炎是一种亚急性特发性间质性肺炎,其特征是斑片状且常为迁移性肺泡实变,对类固醇反应迅速,但复发频繁。急性嗜酸性粒细胞性肺炎可表现为突然而严重的症状,符合ARDS标准,而且可能是特发性的,尽管据报道可确定的原因包括吸烟和吸入暴露物、药物和感染。可能没有血嗜酸性粒细胞增多,但明显的BAL液嗜酸性粒细胞增多(> 25%)是诊断的关键特征。通常在类固醇使用后24-48小时内即可获得快速的临床反应。
实用的诊断方法
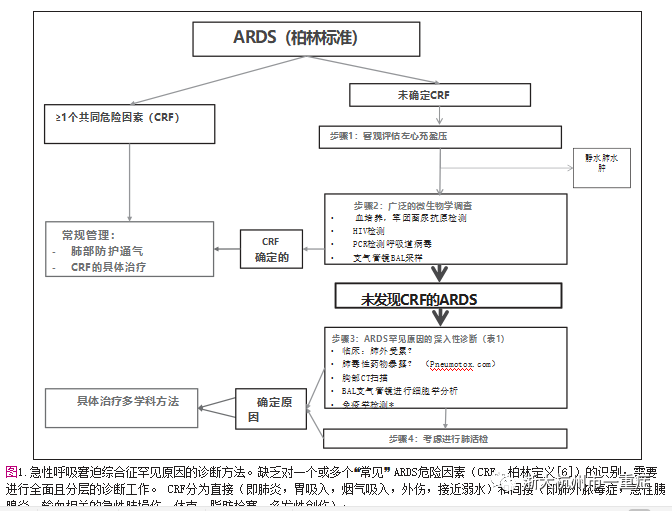
在开始适当的支持治疗后,立即确定ARF/ARDS的原因是个体化患者管理的必要步骤。值得注意的是,在Asteroid研究中,在没有发现ARDS危险因素的ARDS患者中(n= 234名,占整个队列的8.3%),有80%的病人没有诊断出ARDS的原因,没有用任何靶向治疗。出乎意料的是,尽管柏林定义要求,但其中30%的患者并未接受左心充盈压的客观评估。进一步的诊断研究,包括胸部CT扫描、支气管镜BAL检查、免疫学检查和寻找肺毒性药物,分别仅进行了32%、9%、5%和3%的检查。基于常规筛查常见ARDS危险因素的实用诊断方法可以帮助临床医生指出哪些患者发生ARDS罕见病因的风险最高,需要对其进行更全面的诊断检查(图1)。如果未发现ARDS危险因素,则根据最近的建议,需要对左心充盈压进行客观评估,并进行广泛的微生物学检查。其他检查,包括HIV检测、PCR呼吸道病毒检测以及支气管镜BAL采样检查,尤其是在免疫抑制的患者中,将使大量患者被诊断出感染的原因。如果在此阶段诊断检查仍为阴性,则需要使用采用多学科方法:高分辨率的胸部CT扫描成像,支气管镜检查/ BAL(如果没有做),免疫学检查,肺毒性药物。如果存在肉眼可见的BAL液出血且不存在支气管出血,在80%以上的病例中与弥漫性肺泡出血(DAH)有关,如果有肺外症状(例如关节痛,肾脏受累)强烈提示是免疫原因。
如果诊断仍然不清楚,将考虑肺活检方法。先前的观察性系列报道了部分患者中开放肺活检的诊断率很高。具体来说,Libby等人的荟萃分析报告ARDS期间开胸活检的诊断率为84%,其中73%的患者治疗发生了改变。值得注意的是,在最近的一系列研究 中,接受开胸肺活检的ARDS患者中有25%出现并发症,主要包括漏气,但没有死亡归因于手术本身。在美国进行的一项全国性大型研究中, Hutchinson等人报告说,对间质性肺疾病进行了手术肺活检的患者中,医院死亡的危险因素包括开放手术、诊断CTD相关性间质性肺疾病和非选择性手术治疗。但是,应根据具体情况评估开胸肺活检的指征,并且应将其限制在尽管进行了全面检查但仍未做出诊断的情况下。事实上,在LUNG SAFE研究中,在2813例ARDS患者中,只有11例(0.4%)接受了肺活检,这说明绝大多数ARDS病例都没有进行肺活检。
在罕见的急性呼吸衰竭原因患者中开始针对性治疗
ARF罕见病因患者的管理将涉及呼吸科医师、风湿病学家、肿瘤学家以及潜在的多学科方法。详细列出上面列出的所有的具体管理超出了本综述的范围。
对于免疫原因,预防呼吸衰竭的恶化,还需要在出现肺肾综合征时,立即开始免疫抑制治疗,以防止肾脏功能的最终丧失。缓解新发威胁器官或危及生命的ANCA相关血管炎的国际建议是将类固醇静脉注射类固醇(1mg/kg /天,通常需要三次负荷剂量)与环磷酰胺或利妥昔单抗联合使用。关于血浆置换,Jayne等人进行了随机对照研究表明:在患者中表现为肾功能衰竭且血清肌酐水平大于500umol/l,在3个月时血浆置换组的终末期肾脏疾病发生率较低。但是,在长期随访中,两组之间没有统计学差异。尽管当前的指南仍然建议在这种适应症中进行血浆置换,但可以预期PEXIVAS研究的发表将提供明确的答案。除免疫抑制外,血浆置换也是抗GBM抗体疾病患者管理的基石,也是目前唯一可用于预防无尿性急性肾衰竭患者死亡的治疗方法。在大多数情况下,肺部受累的CTD的治疗办法尚不完善,需要类固醇和额外的免疫抑制作用。
药物性肺炎的治疗
要求识别并清除所涉及的药物,严重的需要类固醇治疗,但在这种情况下证据很少。没有有效的疗法可以治疗特发性肺纤维化和急性间质性肺炎的急性加重。在大多数情况下,全身性激素治疗的证据不足。
总体上,未确定ARDS危险因素的患者的预后与具有常见原因的患者的预后没有差异。然而,大多数未发现ARDS危险因素的患者研究有限,其他系列报道的确诊为患有以下疾病的患者,如抗MDA-5抗体治疗的皮肌炎、急性间质性肺炎、IPF急性加重或ARF最后确定为肺恶性疾病则预后较差。在这种情况下,可能需要根据具体情况来考虑是否需要终止或撤消维持生命的治疗的决策,这其中涉及多学科团队和一例一例的个体化讨论。
结论
需要及早发现ARF的病因,以及早开始针对性治疗。没有识别出ARDS共同危险因素的患者应迅速进行全面和分级的诊断检查,以将疾病分类为免疫、药物诱导、恶性或特发性,尤其是ARDS患者。将需要一种多学科的方法,由重症专家和专科专家共同参与,旨在确定哪些患者可以从特定的干预措施(例如免疫抑制,肺毒性药物清除)中受益。

相关阅读
- 11-10 【党支部靓晒】综合3支部:重症医心 温暖有我
- 11-11 准妈妈ICU昏迷一个月,医生:一直隐藏的秘密终于泄露了......
- 10-29 COVID-19流行期间重症监护中的床旁肺部超声
- 10-29 肝硬化患者的自发性细菌性腹膜炎和腹膜外感染(上)
- 10-20 妊高症回顾(上)
- 10-20 妊娠期高血压疾病与心血管疾病相关发病率和死亡率的系统评价分析
- 10-07 经鼻雾化吸入(上)
- 10-07 经鼻雾化吸入(下)
- 10-07 重症患者AKI的生物标志物
- 10-07 重症患者发生AKI增加死亡率?
