CKD患者发生肺动脉高压的诊断与管理


翻译:李沂玮 校对:杨靖
摘要目的
肺动脉高压(PH)是成年慢性肾脏疾病(CKD)中的一种非常普遍且重要的疾病。在这篇综述中,我们总结了PH的定义,讨论了其病理生理学和分类,并概述了CKD相关PH的诊断和治疗。包括用于肾衰竭的肾脏替代疗法。在一般人群中,根据临床表现、病理生理、血流动力学和治疗策略将PH分为5组。在这个分类系统中,尽管潜在有心血管疾病的患者可能占大多数,但CKD相关PH被列入原因不明或机制复杂组。CKD本身可能通过尿毒症毒素、炎症、内皮功能障碍和血管调节改变直接刺激肺循环功能障碍和血管重构。尽管有几项研究统计了慢性肾病和肾衰竭所致的PH有较高的患病率,以及与不良预后的相关性,但对于慢性肾病患者的诊断和治疗策略还没有高质量的证据。在CKD不需要肾脏替代治疗的情况下,容量管理以及对未知的PH危险因素的治疗是至关重要的。在那些需要接受血液透析的患者中,治疗选择有限,如果进行最佳容量管理仍有顽固性低血压,应考虑更换为腹膜透析。
病例
患者,男,60岁,诊断为高血压,2型糖尿病,慢性阻塞性肺疾病(COPD),慢性肾脏病(CKD),根据肾小球滤过率(GFR)和尿微量白蛋白肌酐比分期分层为G4A2期。表现为呼吸急促,持续性腿部肿胀2个月。尽管给予速尿80 mg/d bid治疗并坚持低钠饮食(钠摄入量<2 g / d),但其临床症状仍在进行性加重。静息状态下氧饱96%,活动时92%,查体可闻及P2亢进,吸气相爆破音,下肢膝盖处对称性凹陷性水肿(3mm)。血红蛋白值为11 g / dL,血清白蛋白水平为3.8 g / dL,估测GFR为25mL / min / 1.73 m2。胸部X线检查显示肺容量增加,经胸超声心动图(TTE)显示轻度向心性左室(LV)肥大,左室射血分数为55%,右心室(RV)大小和收缩功能正常,肺动脉收缩压约为50-60mmHg(2年前为35 mmHg)。进而,速尿改为120mg/d bid,并增加美托拉宗(metolazone)5mg/d。由于患者症状持续存在,所以需要进行右心导管检查以准确测量肺动脉压。结果显示,平均心输出量正常,平均肺动脉压(mPAP)为40mmHg,肺毛细血管楔压为20mmHg,提示二型肺动脉高压(PH;即左心疾病所致的肺动脉高压)。因此,改进患者的利尿治疗,并监测了钠的摄入量。
PH定义与分类
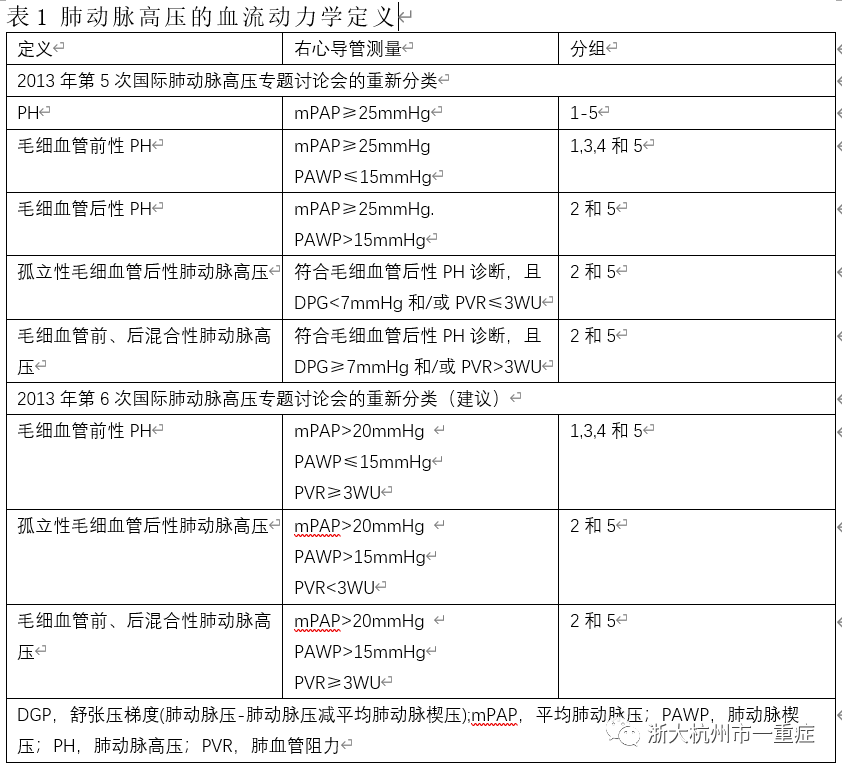
PH(肺循环压力升高)定义为静息状态下,右心导管测量肺动脉平均压≥25mmHg,最近国际工作组提出了改变该阈值20mmHg。健康成年人肺动脉平均14±3mmHg (标准偏差),20mmHg为正常的上限。肺动脉高压(PAH)或1型PH是指在没有某些其他疾病的情况下,限于毛细血管前肺动脉高压的一类PH (本文后面将进一步讨论)。该型无毛细血管后压力升高(肺动脉楔压≤15mmHg),无跨肺循环阻力升高(肺血管阻力>3 Woods单位)。但是,大多数对成年CKD患者的研究未通过右心导管诊断PH,因此,CKD患者的真实发病率和定义改变的作用尚不清楚。
根据临床表现、病理、血流动力学和管理策略,将PH分为5类(BOX1,表1)

PAH(1组PH)
PAH(1组PH)是一种罕见的疾病,估计发病率为成年人2-7例/百万/年,估计患病率为成年人15-60例/百万。肺动脉高压的所有病因都以病理性的肺血管收缩和血管重构为特征。这种增生的血管重构,通常伴有影响所有血管层的肥大和增生,导致血管横断面积的严重减少,增加血流阻力。血管活性分子在PAH的发生发展过程中起着重要的作用,包括内皮素、前列环素、一氧化氮、前列腺素I2、环鸟苷单磷酸等几种具有血管活性(血管舒张或血管收缩)和细胞增殖作用的物质的变化。
治疗上,一般以治疗PH本身为目标,但在某些情况下,如人类免疫缺陷病毒感染,根本治疗是辅助性的。治疗以前列环素、一氧化氮和内皮素为靶点,可改善器官功能状态、血流动力学和生存率。肺移植是万不得已的治疗策略。在1组PH的患者中,肾功能水平下降与死亡率增加有关,其原因可能是因为肾静脉淤血、低心排血量和神经激素激活而导致肾功能下降。用西地那非治疗PAH可增加GFR水平,但其机制和临床相关性仍不清楚。
继发于左心疾患的PH(2组)
由于左心疾患发病率高,所以被认为是PH最常见的原因,其与CKD密切相关。越来越多的研究者认识到,即使积极治疗心衰,也会在早期发生PH,故使得人们对心衰的研究越来越感兴趣。左心功能不全所致的肺静脉压力升高可导致肺动脉和小动脉重构。2组PH可发生于保留射血分数的HF,也可发生于射血分数的下降HF。毛细血管壁的压力性损伤,伴随着肺泡-毛细血管界面的破坏和内皮通透性的增加,是2组疾病的一个显著特征。目前的治疗原则是控制潜在的心脏疾病。
继发于肺部疾患或低氧的PH(3组)
PH可使许多慢性肺部疾病复杂化,包括慢性阻塞性肺病、肺间质病变、囊性纤维化和睡眠呼吸障碍。大多数重度COPD患者会出现PAPs升高,但重度升高并不少见。缺氧性肺血管收缩是一种自适应式机制,限制血液流动到低氧肺泡维持通气-灌注比,并且在慢性肺部疾病中长期存在,导致慢性血管收缩和血管重构,最终导致前毛细血管前闭塞和总毛细管横截面积的大幅减少。治疗的目标是潜在的肺部疾病和逆转低氧血症。慢性阻塞性肺病本身与慢性肾病风险增加有关,可能与糖尿病、氧化应激增加和全身炎症等潜在因素有关。慢性阻塞性肺病和慢性肾病的并存与死亡率的显著增加有关。
慢性血栓性PH(4组)
慢性血栓性PH (CTEPH),即肺动脉血管闭塞导致肺动脉重构,发病率为5例/百万/年。这是一种已知的急性肺栓塞的并发症,但对其发生风险的估计差异很大,在有症状的肺栓塞发生后2年内的发生率从0.1%到9.1%不等。急性血栓栓塞后血栓持续存在,伴有成纤维细胞、结缔组织和小血管病变的组织和浸润是该疾病的特征。肺动脉瓣内膜剥脱术是一种潜在的治疗CTEPH的方法,且需终身抗凝。药物也可用于治疗CTEPH。CTEPH和CKD之间的因果和预后关系仍有待研究。
原因不明的PH,包括肾脏病所致的PH(5组)
这分类除外其余组的疾病,包括原因不明或机制复杂的各类PH。其异质性限制了对发病率和患病率的准确估计。作用机制包括肺血管收缩、血管系统增生性疾病、外在血管压迫和高输出量型HF。合并的全身性疾病包括血液系统疾病(慢性骨髓增生性疾病、脾切除后状态和镰状细胞病)、结节病、甲状腺疾病和肾衰竭。目前尚不清楚如何将因果关系归为肾衰竭,以及如何区分肾功能减退、系统性高血压和轻度心功能障碍的影响。治疗的目标是潜在疾病。
CKD相关PH的流行病学和病理生理过程
流行病学和结局
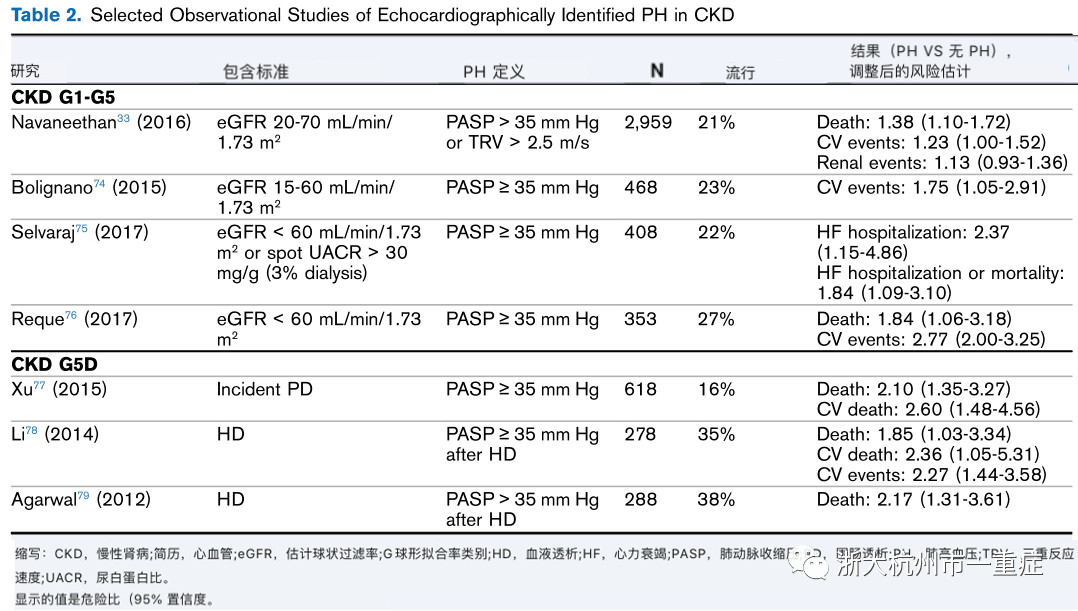
在CKD的几项研究,总结在表2中。2959 例无需KRT的CKD患者中,21%诊断为PH(估计肺动脉收缩压>35mmHg或通过多普勒超声心动图示三尖瓣回流的速度> 2.5m/s[较常用的2.8m/s阈值更为广泛])。PH患病率随着CKD严重程度的增加而增加,从CKD G3a的21%增加到CKD G5的32.8%。通过校正分析,年龄越大,贫血、左室射血分数降低和左室肥厚与PH风险升高相关;估算的GFR与PH发生风险并不是独立相关的。发生PH使死亡率风险增加38%,心血管事件风险增加23%,但并不增加肾脏疾病进展的风险。其他几项研究提供了严重CKD患者的PH发生率的估计值,CKD G5患者为9%到39%,血液透析患者为19%到69%,腹膜透析患者为0%到42%。这种巨大的差异可能反映了测量技术和队列表型的差异。最近的一项荟萃分析显示,2项关于无需KRT的CKD患者的研究(包括CRIC研究),10项关于维持透析(CKD G5D)患者的研究和2项关于肾移植受者的研究表明,PH的存在使死亡风险增加了一倍(相对风险,2.04;95%置信区间[CI],1.71-2.44)。对这些报告特定结果的研究的亚组的荟萃分析表明,PH存在的情况下(死亡率的相对风险为2.20[95% CI, 1.53-3.51],心血管事件的相对风险为1.97 [95% CI,1.45-2.68]),心血管死亡率和心血管事件的风险几乎翻了一番。在患有PAH的人群(1组PH)中,CKD的患病率估计为4%-36%。
很少有研究证实在CKD中利用右心导管证实PH。一项纳入了1873例接受右心导管插入术的CKD患者的单中心回顾性研究显示,大多数患者诊断为毛细血管后疾病(2组与5组一致),占76%的病例,说明2组(或5组)疾病在CKD中占据的优势。最近一项针对3,504例CKD患者的单中心研究发现,毛细血管前联合毛细血管后型PH是最常见、死亡率最高的类型。对62例患有严重CKD (G4、G5或G5D)和呼吸困难(可控制的高血压、心衰伴射血分数降低、瓣膜功能障碍或肺部疾病)的患者进行了单中心研究,他们接受了右心导管测量(接受透析的患者为透析后测量),结果显示,65%接受血液透析的患者为毛细血管后PH,71%患者不需要KRT。13%的血液透析患者为毛细血管前PH,6%的患者不需要KRT。
病理生理学
无需KRT的CKD患者
对于CKD患者合并PH与其他PH患者的病理生理差异知之甚少。在CKD患者中,任何可引起心血管系统疾病的因素,都可通过调节肺血管阻力、左室收缩和舒张功能以及容量过负荷来增加肺压力。与CKD相关的全身血管系统的变化,由继发于CKD的动脉中的纤维和纤维弹性增厚和钙化引起的血管硬化,已经被认为是可能的促成因素。系统性自身免疫性疾病,如系统性红斑狼疮和系统性硬化症是引起肾脏疾病和肺循环疾病的病因。其他可影响弥漫性微血管的疾病,如血栓性微血管病和镰状细胞病,可损害肾脏和肺的微血管系统,引起慢性肾病和PH。引起门脉高压的肝脏疾病可导致PH和肾脏疾病。血管内容量负荷可增加PAPs值,这可能是CKD相关PH的机制之一,在接受透析的患者中,血液透析后PAP显著下降。
CKD本身可能通过尿毒症毒素、炎症、内皮功能障碍和血管调节改变直接导致肺循环功能障碍和刺激血管重构。CKD是一种促炎状态,伴有全身炎症标志物水平升高和氧化应激反应。在CKD患者的体循环动脉中已发现局部动脉炎症,是由循环巨噬细胞的跨内皮迁移而致,这可能也会影响肺循环。除了前面讨论过的,CKD导致PH的许多其他潜在机制还包括贫血、矿物质代谢改变、低蛋白血症和内源性强心类固醇水平升高。这些不同机制的重要性和相关干预潜力将需要广泛的研究验证。PH本身也会影响肾功能。在1组PH(PAH)患者中,肾功能恶化是死亡的独立预测因子,PAH患者通过肾静脉淤血、低心排血量和神经激素活性而降低肾功能。
需KRT的CKD患者
长期以来,人们一直认为用于透析的动静脉(AV)瘘可能对PH有影响,因为它可以增加心输出量,降低肺血管的顺应性,从而导致PAP升高。然而,AVFs在促进PH方面的作用尚不明确,小规模研究的结果相互矛盾。几个小规模研究表明,瘘管血流量与PAP之间没有相关性,在AV瘘管放置和存活后,PAP并没有增加。然而,一项对8例PH患者的研究显示,收缩期PAP在AV通路闭塞时短暂下降。通过AV通路改良或结扎来逆转高输出心力衰竭的报告提供了进一步的证据,表明AV通路在某些情况下可能是重要的。生物不相容透析膜暴露导致嗜中性粒细胞活化,并向肺迁移,是血液透析患者发生PH的另一个潜在因素。在无需KRT的CKD中讨论的所有机制(在前一节中讨论)也适用于透析。
PH的临床表现
PH表现为非特异性的心肺症状,包括呼吸急促、疲劳、胸痛和头晕。最初的症状仅在劳动时出现,休息时出现症状可在疾病晚期时表现出来。进行性右心室功能障碍可引起水肿和腹胀。这些症状可导致功能损害,影响患者的身体、心理和社会健康。当出现其他原因无法解释的呼吸困难,晕厥,或胸痛,必须怀疑PH存在。
CKD相关PH值的诊断和治疗策略
诊断和监测研究
RV异常的心电图结果可发生于PH中,但该参数不够敏感,且不能排除其它诊断。胸片可显示肺动脉高压的特征性表现,如中央型肺动脉扩张伴周围血管的衰减,并可进行其他原因的鉴别诊断。肺功能测试可助于鉴别诊断和评估。多普勒TTE可识别结构性心脏改变导致的PH或由PH导致的结构性心脏改变,并可以估测出PAPs。如果多项超声心动图测量结果与诊断结果一致,则可使用超声心动图对PH作出推断。尽管如此,右心导管测量被认为是有针对性的治疗前的诊断必不可少的。TTE基础上,RV收缩压可通过峰值三尖瓣反流速度和右房压力估计值来估算。在没有肺动脉瓣狭窄的情况下,右心室收缩压与PAP相似。右心室、右心房、下腔静脉和肺动脉的成像,以及肺动脉瓣反流和肝静脉的多普勒超声检查,可以提供诊断证据。


相关阅读
- 11-10 【党支部靓晒】综合3支部:重症医心 温暖有我
- 11-11 准妈妈ICU昏迷一个月,医生:一直隐藏的秘密终于泄露了......
- 10-29 COVID-19流行期间重症监护中的床旁肺部超声
- 10-29 肝硬化患者的自发性细菌性腹膜炎和腹膜外感染(上)
- 10-20 妊高症回顾(上)
- 10-20 妊娠期高血压疾病与心血管疾病相关发病率和死亡率的系统评价分析
- 10-07 经鼻雾化吸入(上)
- 10-07 经鼻雾化吸入(下)
- 10-07 重症患者AKI的生物标志物
- 10-07 重症患者发生AKI增加死亡率?
