急性肺损伤保护性通气策略的病理生理(上)


翻译:孙雁鸣 校对:王剑荣
摘要:
急性呼吸窘迫综合征(ARDS)会导致异质性的肺损伤,这仍然是一个严重的医学问题。仅有的治疗方法之一是机械通气形式的呼吸支持。然而,要使异质性的肺避免机械通气的并发症以及呼吸机相关肺损伤(VILI)是有难度的。ARDS的肺组织的开放依赖于时间和压力,这意味着打开陷闭的肺需要更多的时间和压力,而且在更高的肺泡内压力下,它会更快地重新塌陷。目前的保护性通气策略,ARDSNet的低潮气量(LVT)肺开放方法(OLA)在进一步降低ARDS死亡率方面并不成功。我们推测这是因为LVT策略仅限用于正常组织和局灶性损伤组织混合的肺通气,而OLA虽然设计目的为完全开放和稳定肺,但通常不能成功做到这一点。在这篇综述中,我们分析了VILI的病理生理学。我们还分析了急性损伤肺中呼吸力学的改变,并讨论了这些改变导致VILI的关键机制。我们的分析表明,每次机械通气的通气时,在吸气相和呼气相时,对于维持呼吸力学正常和保护肺部免受VILI的伤害至关重要。动物研究和荟萃分析表明,采用气道压力释放通气模式的时间控制自适应通气(TCAV)方法消除了对异质性损伤肺通气的限制,因为它在开放和稳定时间或者压力依赖性肺方面非常有效。在动物研究中,已经证明,通过用TCAV可以“打开”急性损伤的肺,我们可以(1)通过直接观察胸膜下的肺泡来评估呼气肺容量;(2)通过肺组织的形态计量学分析,评估肺泡情况;(3)观察表面活性蛋白A和B的增加来衡量,来评价正常表面活性物质功能的再生。(4)评估肺顺应性是否增加。
简介:
急性呼吸窘迫综合征(ARDS)最初被认为是一种致命性的双侧肺炎,1967年被Ashbaugh等人定义为一种综合征。不幸的是,自从急性呼吸窘迫综合征被发现以来的50年里,只有少数几种治疗方法被使用,主要是以机械通气的形式支持。但是,受限于异质性肺损伤的限制,机械通气会导致附加的组织损伤,被称为呼吸机诱导的肺损伤(VILI),与肺保护性通气相比可以显著增加死亡率(ARDSNet,2000年)。最初的随机对照试验(RCT)试图通过降低潮气量(Vt)来减少VILI,但未能降低死亡率(Stewart等,1998年;Brower等,1999年)。直到2000年发表的ARDSNet进行了开创性的ARMA研究,才显示死亡率降低。最近的统计和荟萃分析表明,急性呼吸窘迫综合征的死亡率并没有降低到2000年ARMA研究的31%“黄金标准”以下,而是保持在令人无法接受的高水平,高于40%(图1)。尽管有这些令人失望的结果,低潮气量方法的保护性通气策略仍然被推荐为ARDS患者的标准治疗(Fan等,2017,2018年;Papazian等,2019年)。
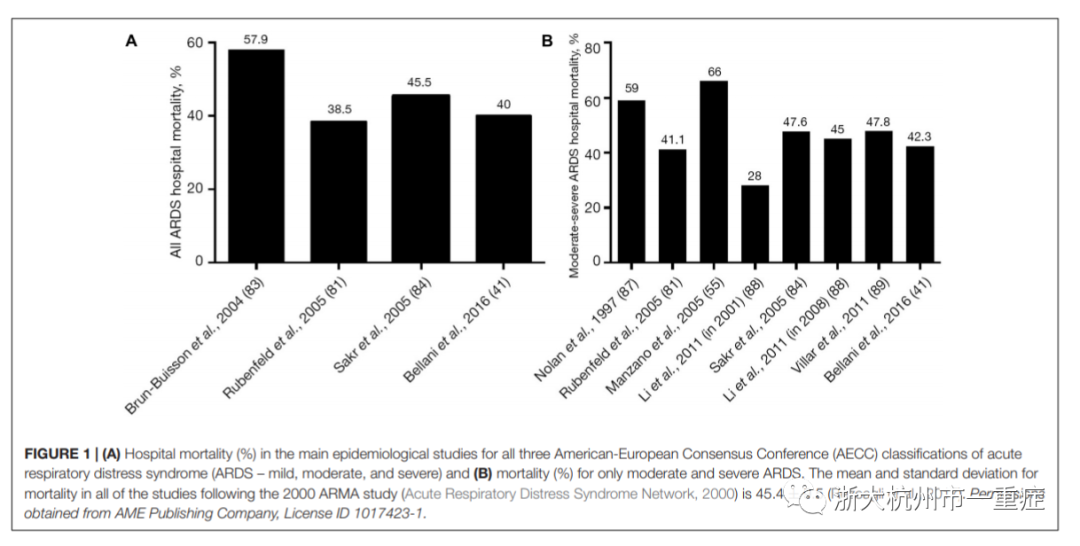
由于ARDS患者的预后数据近20年来没有改善,因此有必要(1)确定机械通气(弹性、粘性或粘弹性)期间肺泡和肺泡管容积动态变化的机制,(2)确定ARDS引起的肺泡力学变化(即机械通气过程中肺泡大小和形状的动态变化)(Grune等,2019年)。(3)确定气道压力和吸气持续时间的作用。(4)以及利用这些知识开发新的通气策略,以更好地减少VILI和保护肺。虽然肺部炎症(生物创伤)在ARDS和VILI的发病机制中也起着重要作用,但本综述的重点将放在通气过程中对组织造成的机械性损伤上。
急性肺损伤的限制性通气
目前的理念是ARDS的肺组织在重力的作用下分成三个区,从而引起异质性损伤(图2)。
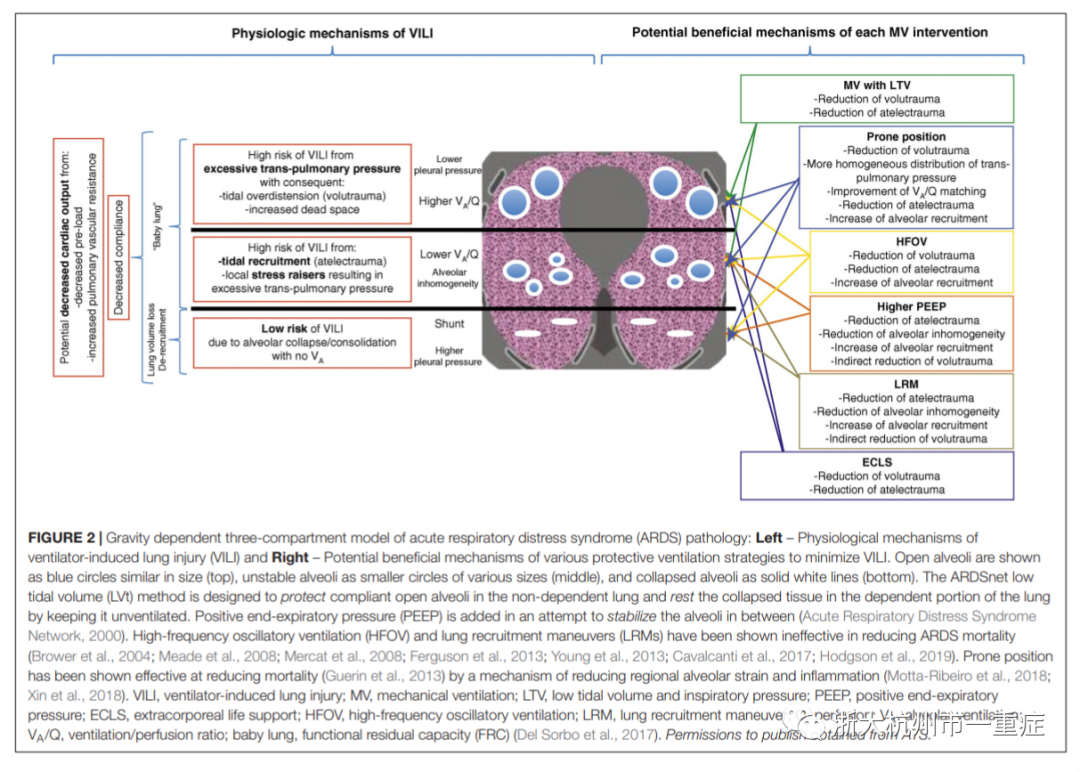
第一个部分,又称非重力依赖区,包含少量正常顺应性的肺泡,在呼气末仍保持充气状态,也被称为“婴儿肺”(Gattinoni and Pesenti,2005)。第二个部分由部分重力依赖区的肺泡组成,这些区域塌陷和/或充满了水肿。第三个区由塌陷的肺泡组成,由于表面活性物质功能的丧失,肺泡仍然处于正常和不稳定之间的过渡区,每次呼吸都会打开和塌陷部分肺泡。
因此,ARDSNet 的保护性通气策略仅限于使用以下三个层次的方法在不引起VILI的情况下对这种异质肺组织进行通气:(1)通过不过度膨胀处于FRC状态的肺组织来保护婴儿肺,(2)通过将重力依赖区的塌陷和充满水肿的肺泡组织保持在通气周期之外来使其休息。(3)以及通过使用经过呼气末正压(PEEP)来稳定组织。
婴儿肺区的保护问题
由于婴儿肺被认为是小体积的正常肺组织(Gattinoni和Pesenti,2005年),它的过度膨胀被认为是VILI的主要机制(Brower等,2004年)。然而,在正常肺承受过高的气道压力(>30 cm H2O)和过高的肺应变(2.5比例),只要过度牵张是静态的,就不会发生过度扩张诱导的VILI。这表明,高容量和高压力的正常组织过度扩张不是VILI的主要机制,除非还存在大的动态应变(Seah等,2011年;Protti等,2013;Jain等,2017年)。婴儿肺的损伤可能不是由于正常组织的过度扩张,而是由于邻近塌陷区域不稳定的肺组织的复张和再次塌陷(Gattinoni等,1995年)。因此,降低Vt和Pplat以减少开放肺组织中的过度膨胀可能不会减少VILI,因为开放的肺组织被大量塌陷和不稳定的低顺应性的组织包围。区域不稳定和炎症反应在整个肺中都发生(包括在计算机断层扫描(CT)或胸部X光中看起来正常的组织中),并作为组织损伤扩大的病理焦点诱导VILI(Wellman等,2014,2016;Cereda等,2016,2017)。因此提示要保护正常肺组织,必须消除区域不稳定性。
然而,其他研究表明,肺过度膨胀是VILI病理生理学的一个主要组成部分(Guldner等,2016年)。Guldner等人在猪ARDS模型中的研究表明,过度扩张的肺比极端肺塌陷导致更多的炎症,这表明应力和应变是VILI的主要机制。虽然这项研究清楚地表明创伤增加了炎症,但没有做组织病理学,也没有以肺重衡量肺水肿的差异。因此,目前尚不清楚炎症反应增加是否会导致任何肺部病变。此外,数据的重新计算显示,容量伤组的平均机械功率为17.12J/min,是肺炎组(7.13J/min)的两倍多(Tonetti等人,2017年)。
其他人还发现,在急性损伤的肺中增加气道压力将以指数级增长的方式导致损伤的快速进展,这支持了Guldner研究中的发现(Hamlington等人,2018年)。综上所述,这些研究表明,在急性损伤的肺组织中,高应力和应变与肺损伤有关,而在正常肺组织中则不是。
肺塌陷区的问题
当肺塌陷低于正常FRC时,充满水肿的肺组织可能产生以下病理生理改变(1)不进行交换气体;(2)容易发展为肺炎(Huynh等,2019年;Li Bassi等,2019年);(3)如果不重新开放,将成为纤维化(Burkhardt,1989;Cabrera-Benitez等,2014;Lutz等,2015);(4)发生呼吸机同步失调(Burkhardt,1989;Cabrera-Benitez等,2014;Lutz等,2015);这与高死亡率有关(Blanch等人,2015);(5)在邻近的开放肺泡和肺泡管中产生应力中心,极大地放大了通气期间施加于这些实质组织的力(Mead等,1970;Gattinoni等,2012年;Cressoni等,2014;Makaksoni等,2014)。研究表明,与肺打开的患者相比,肥胖减肥手术患者中让肺休息会导致更差的氧合,更长的麻醉后重症病房停留时间,以及更多的术后肺部并发症(Talab等人,2009年)。尽管让肺休息这个短语听起来很有保护作用,但并不意味着在塌陷状态下工作是有益的。如上所述,这样的状态与多种病理有关。如果要让肺休息,这意味着要防止肺实质组织受到机械通气的损害,更好的策略是让它处于自然充气状态(Nieman等人,2018年)。
稳定肺区的问题
关于如何最好地设置PEEP以有效稳定肺组织,目前还没有达成共识(Coruch和Luks,2014年;Gattinoni等,2017年;Nieman等,2007a;Bergez等,2019年)。目前用于设置PEEP的ARDSNet方法使用氧分压等级的经验性设置(ARDSNet,2000年),但氧合增加与肺泡稳定性的增加没有很好的相关性(Andrews等,2015年),这是VILI的一个关键机制(Wellman等,2014,2016;Cereda等,2016,2017)。已经使用了许多方法来尝试滴定PEEP以稳定肺组织。这些方法包括使用死腔、肺应力和应变、肺顺应性、CT、压力-容积曲线拐点和电阻抗断层扫描,但目前还没有床边技术来确定设置的PEEP是否确实稳定了肺(Nieman等,2007)。ARDSNet保护、休息和稳定方法的上述问题可能部分解释了在过去20年中ARDS死亡率没有改善的结果(图1)。因为肺塌陷的一致性,保护、休息和稳定。这几乎不可能在不引起某种程度的VILI的情况下进行机械通气。
肺开放策略
肺开放(OLA)的目的是通过使所有三个病理区正常化来消除异质性损伤肺通气的限制问题(图2),目标是使用复张动作(RM)使塌陷的肺组织重新膨胀,并使用适当水平的PEEP使其保持开放。如果能够复张整个肺并防止复发,VILI的主要机械机制(高应变和过度膨胀)将被消除(Nieman等人,2007)。RM是通过提高气道压力(30-40 cm H2O)并将其保持40秒或大幅增加PEEP(25 Cm H2O)并将其与PEEP之上15 cm H2O的驱动压力相结合(Borges等,2006年)。在后一种策略中,PEEP以5cmH2O递增至45cmH2O,直到肺完全复张,当PaO2+PaCO2>400 mmHg时可以确认肺复张(Borges等,2006年)。
在肺复张后,PEEP向下滴定以找到肺再塌陷点(通常通过肺顺应性的急剧下降),然后在第二次复张后,将PEEP设置在塌陷压力之上2 cm H2O。然而,在ARDS患者中测试OLA的多项RCT未能显示出明显优于标准治疗的益处(Brower等,2004年;Meade等,2008年;Mercat等,2008年;Cavalcanti等,2017年;Hodgson等,2019年)。这些失败的原因包括:(1)OLA应用的时机,早期(Borges等人,2006年)VS晚期(Gattinoni等,2006年)](2)一刀切的RM策略,(3)PEEP设置不当无法保持复张的肺开放,(4)复张压力不足以打开所有的肺,(5)存在可复张和不可复张的患者群体(Gattinoni等,2006年)(Gattinoni等人,2006年)。(6)OLA的应用不是作为连续治疗,而是作为一次性事件,两次肺复张间隔过长,或者没有进行再次肺复张。荟萃分析显示,与OLA相关的ARDS相关死亡率没有下降。
为了进一步降低ARDS死亡率和急性肺损伤,必须了解两个病理过程:(1)ARDS使肺易于发生继发性VILI的病理生理学机制;(2)VILI在肺单元(即终末气道、肺泡和肺泡管)中的机制。这些病理生理为保护性机械通气的设计提供了信息,这种通气将通过消除在对不均匀损伤的肺进行通气时存在的限制来允许肺愈合(Nieman等,2018年)。
导致肺损伤的ARDS病理生理
ARDS的四个病理核心
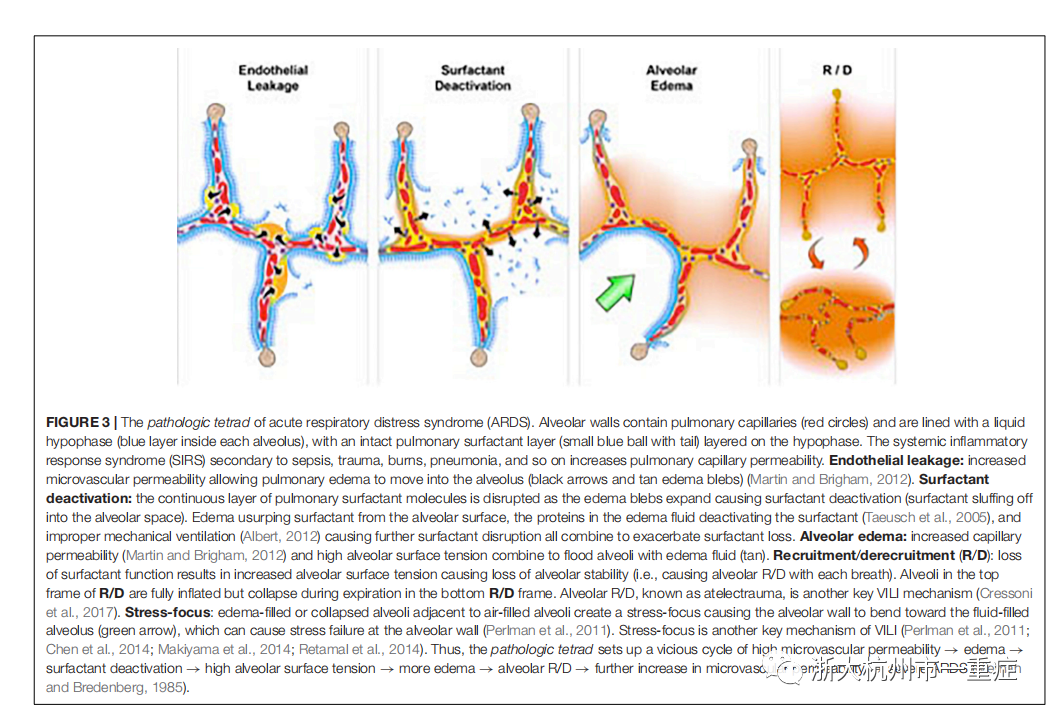
要研究ARDS与VILI的关系,需要了解急性肺损伤的病理基础。虽然ARDS是一种复杂的综合征,但它有四个被广泛接受的中心成分(Thompson等人,2017年),称为“四核心病理”(图3)。四核心包括肺毛细血管通透性增加(图3,内皮渗漏),如果不加以控制,将导致表面活性物质功能的丧失(图3,表面活性物质失活)(Lewis等,1993)。由此产生的高肺泡表面张力将加剧肺泡通透性的增加(图3,肺泡水肿)(Nieman和Bredenberg,1985)。表面活性物质功能障碍会改变肺泡力学,导致每次呼吸时的肺泡再膨胀/萎陷(R/D)(图3,R/D)(Schiller等,2001年)。四的每一个组成部分都对肺泡力学有深远的影响。表面活性物质失活通过促进异质肺组织的不稳定和塌陷,为继发性VILI奠定了基础。此外,在塌陷区域,II型细胞的表面活性物质分泌将受到抑制(Wirtz和Dobbs,1990;Majudar等,2012年)。肺表面活性物质分泌减少会使肺泡水肿所致的已经降低的表面活性物质功能恶化并持续存在。

相关阅读
- 11-10 【党支部靓晒】综合3支部:重症医心 温暖有我
- 11-11 准妈妈ICU昏迷一个月,医生:一直隐藏的秘密终于泄露了......
- 10-29 COVID-19流行期间重症监护中的床旁肺部超声
- 10-29 肝硬化患者的自发性细菌性腹膜炎和腹膜外感染(上)
- 10-20 妊高症回顾(上)
- 10-20 妊娠期高血压疾病与心血管疾病相关发病率和死亡率的系统评价分析
- 10-07 经鼻雾化吸入(上)
- 10-07 经鼻雾化吸入(下)
- 10-07 重症患者AKI的生物标志物
- 10-07 重症患者发生AKI增加死亡率?
