CPR和ECMO:下一个前沿(上)


翻译/总结:曾小康 校对:席绍松
摘要
心肺复苏(CPR)是心脏骤停的一线治疗方法,体外膜氧合(ECMO)传统上被用作对抗循环衰竭的手段。然而,新的进展表明CPR和ECMO可以作为互补用于心脏骤停。这篇综述详细介绍了新兴的科学、技术和临床应用,使这些循环支持模式成为心脏骤停的新范式。
正文:
心脏骤停
心脏骤停的定义是心脏失去机械活动,导致前向血流的突然丧失。这导致重要器官的灌注明显减少或消除,如果循环系统不能重新恢复,就会迅速导致死亡。美国每年有超过35万的院外和超过20.5万的院内心脏骤停患者,心脏骤停占心脏死亡总数的60%以上。心脏骤停的初始节律包括心室颤动、无脉性室性心动过速、无脉性电活动(正常电活动,但心功能不全或极低)和心搏停止。对付所有这些节律的最初方法包括启动心肺循环。
CPR优势和局限性
复苏的一个主要指导原则是增加复苏过程中产生的前向血流量,增加存活的机会。心肺复苏术(CPR)与除颤联合治疗可休克性心律失常(室颤和无脉性室性心动过速),可消除致命心律失常,恢复复苏过程中的血流。CPR的一个主要组成部分是应用胸部按压来增加胸内压,进而增加平均血压和促进血液流动。然而,所提供的压缩的质量可能因提供者的物理能力而不同。救援者疲劳是人工心肺复苏的一个局限性,但可以通过频繁更换提供者来缓解,或者,在可能的情况下,使用自动化设备,也可以提供更一致的按压。在复苏过程中增加血流量的其他方法,如腹部捆绑也被研究过,可能是有益的,尽管它们尚未被纳入临床实践。除了机械方法外,标准方案包括使用肾上腺素和抗心律失常药物来增加外周血管抵抗,消除心律失常,并提高平均血压。然而,尽管在技术和技术上有差异,CPR的总体成功率在10%到20%之间,并且经常伴有肺水肿、肋骨断裂、胃扩张和胸骨骨折。
ECMO基本原则
体外膜氧合(ECMO)是一种机械循环支持形式,它由体外血泵和氧气发生器组成。ECMO技术传统上用于各种心肺状况,最近被用于心脏骤停。
ECMO有两种常见配置,可以针对性的设置参数。一般来说,对于氧合受到影响的呼吸支持,如严重反复发作的急性呼吸窘迫综合征,静脉-静脉ECMO (VV-ECMO)可用于从静脉系统中取出缺氧的血液,通过氧合器,然后通过静脉系统将氧合的血液返回到循环中。然而,在心力衰竭的情况下含氧血液在这期间不能充分循环到全身,可以通过额外的支持来达到(VA-ECMO)(图1)。即静脉血从静脉系统中引出,然后通过有足够压力的氧合器,从外周血管(通常是股动脉)回输到体内,保证终末器官的灌注流量恢复。
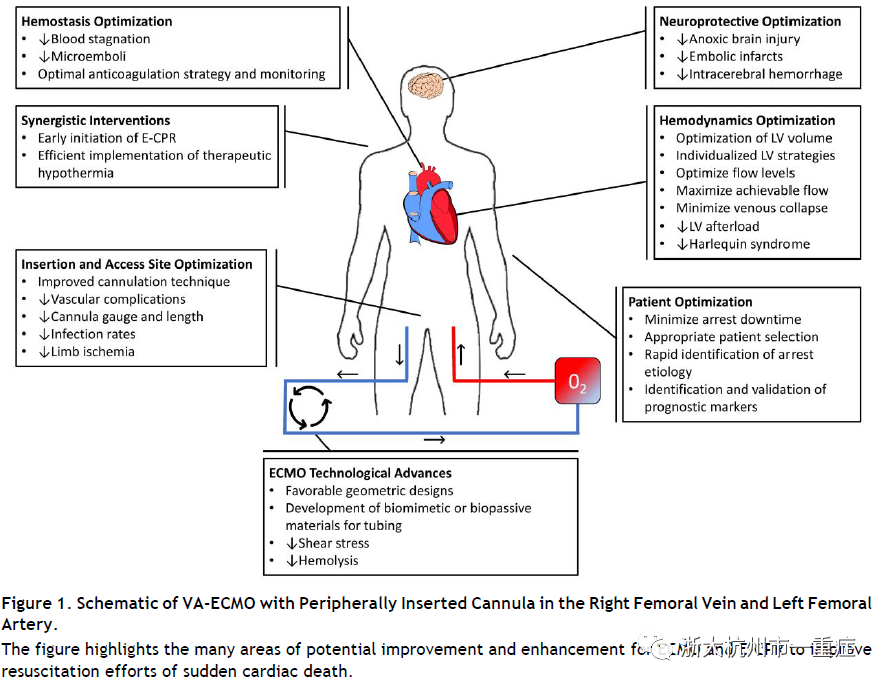
目前,ECMO的启动和管理是很麻烦的,因为它需要熟练和有经验的提供者进行插管,以及系统抗凝治疗,并需要一名灌注师进行床边管理。当应用于难治性心力衰竭时,ECMO在儿科患者和成人患者中的存活率分别接近60%和40%。与ECMO相关的不良事件包括手术和套管部位出血、感染、肾功能衰竭、高胆红素血症和氧合器机械故障。其他常见的并发症包括血栓和纤维蛋白淤积、溶血、空气栓塞、左心室负荷过重、南北综合征和肢体缺血。
ECMO用于心脏骤停和体外CPR
最近的研究发现,当有适当的资源可用时,ECMO是传统CPR在心脏骤停情况下的一种合理的替代方法。使用VA-ECMO治疗由于心脏机械活动减弱而突然失去脉搏的患者被称为体外CPR (E-CPR)。以往发表的研究通常基于出院生存率和长期神经功能评估E-CPR的有效性,其中院外心脏骤停(OHCA)和院内心脏骤停(IHCA)被独立考虑。
体外膜氧合(ECMO)可用于心脏骤停时心脏鲜有或无内在活动时的血流恢复。应用于心脏骤停时,ECMO可以使患者的生存率提高一倍,即使在停搏50分钟后。此外,最近的一项研究表明,在停搏后30分钟内开始ECMO的患者生存率为100%,在75分钟内开始ECMO的患者生存率为25%。值得注意的是,在88例经历IHCA的患者中,常规CPR (C-CPR)的平均持续时间为13分钟(n=48),而复苏失败的平均持续时间为28分钟(n= 40)。
E-CPR和C-CPR的比较
与C-CPR相比,证据通常支持E-CPR的使用。然而,证据各不相同。一个系统回顾25例观察研究得出的结论是,由于低质量的证据,E-CPR和C-CPR在研究中没有明显的优势。而另一项研究表明,在OHCA时,E-CPR和C-CPR的存活率相似。相相反,一项荟萃分析显示,与C-CPR相比,E-CPR提高了生存率和良好的神经系统结果,尤其是停搏后3 - 6个月。另一项对2260名患者的荟萃分析也基于出院生存率和远期神经功能情况,支持E-CPR而不是C-CPR。在另一项531例患者的单次研究中,有38例患者因非休克性OHCA接受了E-CPR,结果发现E-CPR组的生存期和脑功能结果均高于C-CPR组。在一项对454名OHCA患者的前瞻性观察研究中,与接受C-CPR治疗的患者相比,接受E-CPR治疗的患者在停搏后1个月和6个月的良好神经系统评分显著高于接受E-CPR治疗的患者。通过对前瞻性观察队列数据的事后分析,48例OHCA患者倾向匹配,E-CPR组的完整生存期明显高于C-CPR组。在一项406例IHCA患者的回顾性观察研究中,有30例患者的倾向匹配,同样发现E-CPR相对于C-CPR有生存优势。
E-CPR用于OHCA和IHCA
比较E-CPR对OHCA和IHCA的有效性的研究尚无定论。对15项OHCA研究和7项IHCA研究的系统回顾表明,两组均没有证据支持或否定E-CPR的使用。另一项对77例患者的研究发现,IHCA患者的结果比OHCA患者更好,但这种差异是由患者因素和E-CPR启动时间延迟造成的。423例接受E-CPR的患者中,尽管后者从昏迷到E-CPR的时间显著延长,但IHCA组的良好神经系统转归率(34%)明显高于OHCA组(9%)。在85例非心脏术后患者中,33例IHCA组(42%)和OHCA组(15%)的生存期差异更为显著;然而,IHCA组的C-CPR持续时间明显缩短,这一发现更为复杂。
一项对顽固性OHCA的系统回顾发现生存率为22%,神经系统恢复率为13%,这与260例E-CPR神经系统恢复率为12%相当。一项对525例E-CPR OHCAs的前瞻性登记研究报告生存率为8%。一项涉及258例E-CPR OHCAs的多中心回顾性研究发现,重症监护病房(ICU)生存率为24%,19%的神经系统预后良好。此外,一项涉及20例心室颤动的E-CPR OHCAs的回顾显示,自发循环(ROSC)持续恢复95%,出院时生存率50%,出院后1年生存率50%,出院时神经功能正常40%。一项有1796名E-CPR OHCA患者参与的队列研究报告,到出院时生存期为29%,而在整个队列中生存期没有显著变化;这与24例E-CPR OHCA患者的倾向匹配研究中描述的比率相似。
E-CPR成功的预测因素
患者类型、复苏时间和病人的年龄可能是E-CPR结果的决定因素。以65岁为基础,停搏并接受现场CPR,无重大合并症,并在停搏后1小时内启动ECMO治疗的患者,神经系统预后可能改善20%。25例类似的研究报道44%拥有良好的神经功能恢复,病人选择基于停搏的心脏或肺引起,心跳骤停一直被目击,胸外按压在10分钟内开始,最初的节律是心室纤颤或室性心动过速,有机械CPR设备与医护人员,从心跳骤停到达医院不到60分钟。这些严格选择患者的发现被一项荟萃分析所强化,该荟萃分析发现,当进行人工心肺复苏超过30分钟时,生存率呈负趋势,另一项研究中,当心脏骤停超过40分钟后,神经系统存活率从30%下降到15%。在另一项研究中,病人年龄也与1个月的存活率降低减少有关,该研究得出结论,70岁以上的病人可能不适合接受E-CPR。
E-CPR预后标志物的识别和验证对患者的选择有价值。然而,一篇综述明确指出,OHCA后E-CPR的预后指标不可用,而另一篇综述则将心脏节律、目击事件和可逆的停搏原因描述为有利的预后因素。其他决定脑功能预后好坏的独立因素可能还包括E-CPR的使用和从心跳骤停到住院的时间。一项对10名OHCA患者的研究表明,瞳孔直径≥6mm可能是一种预后不良指征。
ECMO应用的局限性
资源需求
虽然ECMO的机械循环支持仍然是一种有希望提高复苏效果的治疗方法,但目前ECMO资源密集,发病率高,限制了更广泛的应用。在ECMO中需要一个灌注师来启动、消除泡沫和管理系统,而这在紧急情况下通常是不可行的。外科医生需要放置大口径套管,使静脉引流和允许足够的血流,也可能不是即时可用的。此外,大插管会增加血管并发症,特别是插入部位的肢体缺血和出血。套管的大小在儿科中更为重要,在儿科中,由于相对动脉狭窄,使用小套管可能会限制足够的血流。
专业知识与培训
目前,ECMO专家的培训和继续指南建议医生要“成功地完成临床专家的机构培训要求”。因此,对于打算在患者身上使用ECMO的医生并没有普遍的要求。虽然这是有益的,因为它的限制较少,可能会有利于患者进一步接受ECMO治疗,但如果没有丰富的外科/介入/ECMO经验的医生遇到设备和管理相关的并发症时,它可能是有害的。
ECMO有效性
从2006年到2011年,美国成年人使用ECMO的人数增加了433%,全球范围内也出现了类似的趋势,从1986年到2015年,随着执行率提高,适应证标准扩大,体外生命支持组织(ELSO)报告的数量增加了5倍。然而,ECMO仍然主要在城市地区的大型学术医疗中心提供。尽管如此,随着ECMO变得更加可用,ECMO使用的传统限制因素(如人员时间和成本)将会减少。随着ECMO可用中心的数量和适应症的增加,有望继续改进。
使用ECMO的知识缺口
如果能够填补这些知识的空白,ECMO在未来的成功率将会大大提高,尤其是在应用于心脏骤停的时候。
灌注充足的决定因素
VA-ECMO的目的是提供足够的灌注,以实现血流动力学的稳定,恢复和维持重要器官的氧合。在评估ECMO血流时,必须考虑各种血流动力学参数。为了达到正常的动脉氧合,ECMO流量一般需要达到正常心输出量的60%。这是通过使用各种类型的血泵来实现的,这些血泵提供压力来驱动血液通过电路。因此,每分钟转数(RPM),流量(L/min),流入和流出压力,和混合静脉血氧饱和度(SvO2)都需要积极监测。这些参数的变化可以表明电路的内在和外在问题。例如,在设定一个稳定的RPM时,流速下降可能反映了前负荷减少(低血容量、出血、张力性气胸)或后负荷增加(膜血栓、动脉插管扭结或系统血管阻力升高)。
平均动脉压(MAP)是灌注的另一个指标,在所有血流动力学受损的患者中都要仔细监测。MAP可以粗略地近似为舒张压和收缩压的函数,也可以替代心输出量、中心静脉压和全身血管阻力。在VA-ECMO中,MAP是由自身心功能和电路泵输出的组合决定的,它可以根据相对驱动力有无脉动发生。因此,血流是根据多种参数来调整的,包括MAP、本身的心功能、全身性血管阻力,或需要正性肌力药物或其他机械循环支持装置的额外支持。VA-ECMO起始血流速为30ml /kg/min(理想体重),理想的中心静脉血氧饱和度为70%。然而,一般成人靶灌注为60 ml /kg/min。气体流量,也被称为气体清除,控制二氧化碳的清除量,并被调整以保持血液pH值和二氧化碳分压分别为7.40和40 mmHg。在评估最佳全身灌注的可用参数中,最客观和临床相关的是氧饱和度(SpO2)和乳酸水平,因为它们与组织灌注直接相关。理想的设置将有利于平衡氧的输送和吸收,维持静脉血氧饱和度70%和血清乳酸水平低于2.2 mmol/L或趋于正常。如果在ECMO支持下SvO2和乳酸不能在合理的时间内恢复,则可能是ECMO动力不足(例如脓毒症高心排休克时),或者可能是氧输送不充分,这可能需要增加流量或输血。
尽管灌注的血流动力学和生理指标对ECMO管理策略至关重要,但仍有很大的局限性。首先,这些指标是基于人口平均水平,因此可能不适用于个别病人。其次,这些指标是针对全身生理的,因此不能代表一个特定的器官需要什么,而不是它正在接受什么。最后,氧和血流量输送需求可能会因许多因素而改变,如CPR和ECMO病人的躁动和血液分流到肠道(如果病人在ECMO时可以吃东西的话)。虽然后者与ECMO应用于心脏骤停无关,但所有这些局限性都源于不知道组织灌注水平、器官特异性、以及实时的氧供氧耗关系。
明日待续。。。。。。。


相关阅读
- 09-13 第八期“浙大市一.临床大讲堂”预告
- 05-24 2021年第三届湖畔眼底病高峰论坛暨浙江省级继续医学教育项目《玻璃体视网膜疾病诊疗进展》圆满举办
- 10-29 COVID-19流行期间重症监护中的床旁肺部超声
- 10-29 肝硬化患者的自发性细菌性腹膜炎和腹膜外感染(上)
- 10-20 妊高症回顾(上)
- 10-20 妊娠期高血压疾病与心血管疾病相关发病率和死亡率的系统评价分析
- 10-07 急性心梗后超声可发现的机械性并发症
- 10-07 做了一回赵半仙--高血压心脏病
- 10-07 综合生命支持降低暴发性心肌炎死亡率的多中心研究(上)
- 10-07 经鼻雾化吸入(上)
